Une avancée majeure contre le cancer : la tumeur au cerveau d’une patiente réduite de 80% en 5 jours
Dans l’univers impitoyable de l’oncologie, une découverte exceptionnelle vient bouleverser notre compréhension du traitement des tumeurs cérébrales. Une tumeur cérébrale parmi les plus agressives au monde a pratiquement disparu en seulement cinq jours grâce à une thérapie révolutionnaire. Cette avancée médicale majeure, testée aux États-Unis, ouvre des perspectives inédites pour les patients atteints de glioblastome et leurs familles.
La Thérapie CAR-T : Une Innovation Technologique de Pointe
Principe Fondamental de l’Immunothérapie Cellulaire
L’immunothérapie CAR-T (Chimeric Antigen Receptor T-cell) représente l’avant-garde de la médecine personnalisée. Cette technologie médicale de pointe consiste à prélever les lymphocytes T du patient, les modifier génétiquement en laboratoire pour qu’ils reconnaissent spécifiquement les cellules cancéreuses, puis les réinjecter dans l’organisme.
Processus de traitement innovant :
- Prélèvement des cellules immunitaires du patient
- Modification génétique en laboratoire spécialisé
- Multiplication cellulaire contrôlée
- Réinjection des cellules « entraînées »
- Activation du système immunitaire contre la tumeur
Adaptation Révolutionnaire pour les Tumeurs Cérébrales
L’équipe du Massachusetts General Hospital a développé une version révolutionnaire de cette thérapie, spécifiquement adaptée aux défis uniques des tumeurs cérébrales. Cette innovation combine la thérapie CAR-T traditionnelle avec des anticorps monoclonaux supplémentaires, créant une approche thérapeutique double particulièrement efficace contre le glioblastome.
Caractéristiques techniques avancées :
- Ciblage précis des cellules tumorales cérébrales
- Franchissement optimisé de la barrière hémato-encéphalique
- Réduction des effets secondaires neurologiques
- Activation immunitaire localisée
- Durabilité thérapeutique prolongée
Résultats Cliniques Exceptionnels
Cas Clinique Remarquable : Disparition Complète en 5 Jours
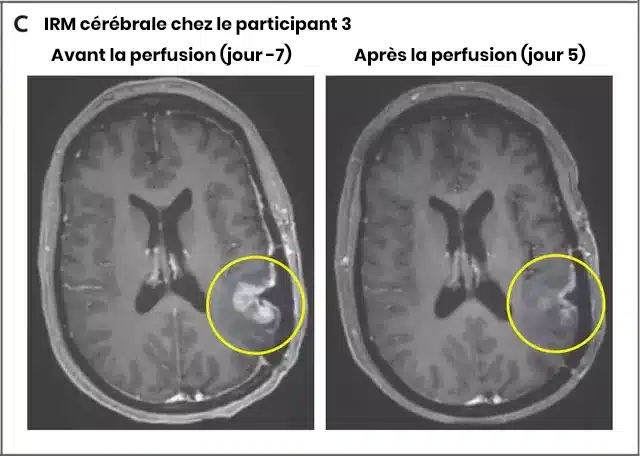
L’essai clinique, mené sur trois patients volontaires, a produit des résultats spectaculaires qui dépassent toutes les attentes médicales. Le cas le plus impressionnant concerne une patiente dont la tumeur a pratiquement disparu après une seule perfusion du traitement expérimental.
Progression thérapeutique documentée :
- Jour 1 : Administration du traitement CAR-T modifié
- Jour 2 : Première réduction tumorale observable (18,5%)
- Jour 5 : Régression quasi-totale de la masse tumorale
- Semaine 8 : Réduction de plus de 60% du volume tumoral
- Suivi à long terme : Maintien de la rémission
Analyse Comparative des Résultats
Cette efficacité thérapeutique contraste dramatiquement avec les traitements conventionnels du glioblastome, où la survie médiane dépasse rarement 15 mois. Les résultats préliminaires suggèrent une révolution dans la prise en charge de ces tumeurs particulièrement agressives.
Comparaison avec les traitements standards :
- Chirurgie : Résection partielle souvent impossible
- Radiothérapie : Efficacité limitée sur les récidives
- Chimiothérapie : Toxicité importante, résultats modestes
- Immunothérapie CAR-T : Régression massive et rapide
Mécanisme d’Action et Innovation Scientifique
Ingénierie Cellulaire de Précision
La technologie développée par l’équipe du Dr Bryan Choi repose sur une ingénierie cellulaire sophistiquée. Les lymphocytes T modifiés expriment des récepteurs chimériques spécifiquement conçus pour reconnaître les antigènes présents sur les cellules de glioblastome.
Processus d’ingénierie cellulaire :
- Identification des antigènes tumoraux spécifiques
- Conception de récepteurs chimériques sur mesure
- Transfection génétique des lymphocytes T
- Validation fonctionnelle in vitro
- Optimisation de la production cellulaire
Approche Thérapeutique Combinée
L’innovation majeure réside dans la combinaison de deux stratégies thérapeutiques complémentaires. Cette approche synergique permet d’attaquer la tumeur sur plusieurs fronts simultanément, maximisant l’efficacité tout en minimisant les risques de résistance.
Stratégies thérapeutiques intégrées :
- Activation immunitaire spécifique anti-tumorale
- Ciblage moléculaire précis des cellules malignes
- Stimulation de l’immunité naturelle du patient
- Prévention des mécanismes d’échappement tumoral
- Maintien de la surveillance immunitaire
Perspectives d’Avenir et Développement Clinique
Expansion des Essais Cliniques
Fort de ces résultats encourageants, l’équipe de recherche prépare l’expansion de ces essais cliniques à une cohorte plus large de patients. Cette phase d’élargissement permettra de confirmer l’efficacité et d’évaluer la sécurité du traitement sur un échantillon représentatif.
Prochaines étapes de développement :
- Essais cliniques de phase II sur 50-100 patients
- Études de toxicité et d’effets secondaires
- Optimisation des protocoles thérapeutiques
- Développement de biomarqueurs prédictifs
- Préparation des dossiers réglementaires
Applications Thérapeutiques Élargies
Cette innovation pourrait révolutionner le traitement d’autres tumeurs cérébrales primaires et métastatiques. Les chercheurs explorent déjà l’adaptation de cette technologie à d’autres cancers du système nerveux central.
Cancers cérébraux ciblés :
- Astrocytomes de haut grade
- Oligodendrogliomes anaplasiques
- Médulloblastomes récidivants
- Métastases cérébrales multiples
- Tumeurs pédiatriques du cerveau




